



Ligações covalentes simples são formadas quando dois átomos compartilham uma aresta, como na estrutura C abaixo. Isso resulta na troca de dois elétrons. Ligações iônicas são formadas pela transferência de um elétron de um cubo para outro, sem compartilhar uma aresta (A). Um estado intermediário B, onde apenas um canto é compartilhado também foi postulada por Lewis.
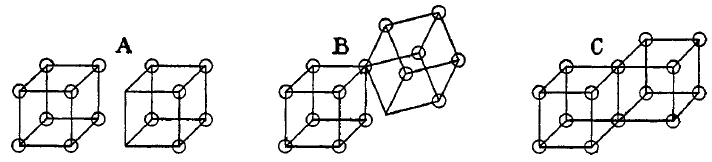
Ligações duplas são formadas pelo compartilhamento de uma face entre dois átomos cúbicos. Isto resulta no compartilhamento de quatro elétrons:
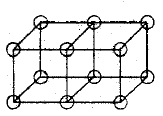
Ligações triplas não podiam ser explicadas pelo modelo do átomo cúbico, porque não há nenhuma maneira de dois cubos compartilharem três cantos.
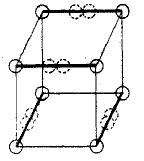
Lewis sugeriu que os pares de elétrons em ligações atômicas têm uma atração especial, o que resulta em uma estrutura tetraédrica, como npróxima figura (a nova localização dos elétrons é representado pelos círculos pontilhados no meio das bordas grossas).
Isto permite a formação de um vínculo único, através da partilha de um vértice, uma ligação dupla, compartilhando uma aresta e uma tripla ligação através da partilha de uma face do cubo.
Ele também reproduz a rotação livre em torno de ligações simples e também a geometria tetraédrica do metano.
Extraordinariamente, pode-se dizer que havia um grão de verdade nesta ideia, porque mais tarde foi mostrado que os resultados do princípio da exclusão de Pauli resultam em um "buraco de Fermi" cuja repulsão decresce entre um par de elétrons com spins opostos no mesmo orbital.
Como essa teoria teve o mérito de explicar a ligação covalente sem recorrer a conceitos complicados da mecânica quântica, foi logo aceito e é ensinado até hoje nas escolas. O problema é que ele falha em explicar compostos de Boro e/ou compostos que aceitam mais do que 8 elétrons na camada de valência.
Isso faz com que muitos professores, apegados ao que eles chamam "regra do octeto", preferem esconder as exceções para não estragar a beleza da tal regra. Só que ela não é uma lei, é uma regra, baseada em uma teoria parcialmente bem sucedida. Não podemos negar a elegância da proposição de Lewis, mas também não podemos atribuir-lhe um caráter de infalibilidade.
Ensinem a teoria de Lewis, mas evitem usar esse termo "regra do octeto", e familiarizem-se com a história da ciência que vocês (eu inclusive) se dedicam a ensinar para evitar de propagar conceitos errôneos.
Para os mais curiosos, o artigo original de Lewis foi publicado aqui:
01/04/1916. "THE ATOM AND THE MOLECULE.
Journal of the American Chemical Society 38 (4): 762–785.
doi:10.1021/ja02261a002
FONTES: Wikipedia1, Wikipedia2, História da Química - Um livro-texto para a graduação














O Hubble, primeiro telescópio espacial, que revolucionou a astronomia e a compreensão do universo ao transmitir mais de 750.000 imagens espetaculares dos confins do universo, completa neste fim de semana 20 anos de lançamento.

O telescópio foi lançado em 24 de abril de 1990 acoplado ao ônibus espacial americano Discovery, que o colocou em órbita a 600 km de altitude. No entanto, devido a algumas falhas no espelho do telescópio, ele só foi colocado em funcionamento três anos mais tarde.
O telescópio de 12 toneladas e 13,3 metros de comprimento fez 900.000 instantâneas, que permitiram obter 570.000 imagens de mais de 30.000 objetos celestes, alguns deles nos confins do universo.
Graças a ele, os físicos conseguiram confirmar a existência da "matéria escura", que até então era uma hipótese (o cosmos é formado por quase de 5% de matéria visível e 20% de matéria esscura).
Devido à alta resolução das imagens obtidas com o auxílio do Hubble, pequenas proto-galáxias da época em que o universo tinha menos de um bilhão de anos foram assinaladas e a idade do universo pode ser estimada em torno de 13,7 bilhões de anos.
Ah, e uma grande dúvida da ciência foi respondida: o universo está em expansão, sim.
"Sem dúvida nenhuma, o Hubble é o instrumento científico mais reconhecido e que deu o maior número de êxitos científicos da historia da humanidade", afirma Ed Weiller, alto funcionário da Nasa.
A missão do ônibus espacial Atlantis permitiu prolongar em pelo menos cinco anos a vida útil do Hubble, à espera do sucessor, o ainda mais telescópio espacial infravermelho "James Webb Space Telescope (JWST)", que tem o objetivo de jogar luz sobre o momento da origem do universo.
O Google, que não é bobo, marcou a data com um logotipo especial na página do seu buscador.

Só nos resta agradecer a esse artefato científico, fruto da engenhosidade humana. Outra hora eu escrevo um pouco mais sobre quem foi a personalidade que emprestou seu nome ao telescópio.
FONTE: Jornal do Brasil Online
Hoje é o dia da Terra, ou Earth Day para os íntimos.

Lá no site http://www.earthday.org/ você pode acompanhar toda a movimentação mundial em prol do planeta em todos os lugares em que vai acontecer alguma atividade pública,
E já que o tema de hoje é esse, vamos puxar a brasa para o meu assado que é a físico-química.
Li um artigo bem interessante nesse site aqui ó LINK. O autor fala sobre o fenômeno da tensão superficial. E o que isso tem a ver com o dia da Terra?
Acompanhem o raciocínio comigo:

Moléculas no interior do líquido (água, no caso) apresentam isotropia (ou quase isso) de forças. Em palavras de seres humanos normais, as forças de atração intermoleculares são igualmente distribuídas pelo espaço.
Já as moléculas na superfície do líquido conseguem interagir apenas com moléculas ao lado e abaixo de si, porém interagem muito pouco com outras moléculas acima de si, visto que são raras as moléculas presentes na fase gasosa.
Se você observar bem a figura acima, notará que ocorre um desequilíbrio de forças nas moléculas da superfície, fazendo com que a força resultante seja direcionada para o interior do líquido.

O resultado disso? Forma-se um filme superficial de liquido, uma película. Ela é bem forte, pode suportar o peso de um pequeno inseto sobre ela, às vezes até mesmo um clip de papel pode ser colocado com cuidado sobre o filme superficial sem que ele se rompa.
A tensão superficial é responsável pelos líquidos formarem gotas esféricas, o que determina se o líquido vai ou não molhar uma superfície tem relação também com a tensão superficial. A água, por exemplo, vai espalhar-se bem em superfícies polares, e vai tender a formar gotículas quase-esféricas em superfícies apolares.
A adição de um surfactante (vamos dizer, por exemplo, um detergente líquido) à água faz com que o filme superficial perca coesão. Como resultado disso, a água torna-se mais "molhada", ela se espalha mais do que sem a presença do detergente.
Isso é bem útil quando queremos que a água dissolva uma superfície gordurosa (como aquelas que ficam sobre os pratos que usamos em nossa alimentação). O detergente dissolve a gordura do prato e a água ajuda a carregar a sujeira removida pelo detergente.
Justamente essa tecnologia que nos ajuda a manter nossos utensílios de alimentação limpos é a causa de muita preocupação por parte das pessoas preocupadas com o ambiente terrestre.
O uso indiscriminado de detergentes semi-biodegradáveis faz com que a tensão superficial das águas diminua consideravelmente.
O despejo de nossos resíduos domésticos nos rios e lagos faz com que a água não seja mais um ambiente propício aos pequenos insetos, visto que eles não conseguem mais caminhar sobre o filme superficial com tanta facilidade.
Isso faz com que a reprodução desses pequenos seres seja ameaçada, gerando um desequilíbrio ecológico sem precedentes.
Além disso, certas substâncias presentes nas embalagens plásticas são despejadas nos mesmos rios e lagos e afetam negativamente os ciclos hormonais de pequenos anfíbios e mamíferos que bebem ou vivem nessas águas contaminadas.
Vejam, não quero alarmar ninguém com essa reflexão, mas no dia dedicado ao nosso planeta, nada melhor do que falar abertamente de um problema que certamente não vai parar de cresces enquanto continuarmos a usar indiscriminadamente produtos de limpeza pouco ecológicos.
Uma solução paliativa seria passar a usar o sabão em barra para lavar as louças, ele é menos efetivo que o detergente líquido mas é completamente biodegradável e afetaria em menor escala as águas.
Bom, vou parar de filosofar por aqui, desejo um dia de profundas reflexões a todos os terrestres (e se tiver algum leitor marciano que acessa o blog também sugiro que leia o texto todo e use nas suas salas de aula marcianas).
Abraços digitais!
GAUTO, Marcelo;
; acessado dia 13/04/2010.




O jogo em questão originou-se de uma tese sobre design de jogos de autoria de Jenova Chen. flOw é um jogo baseado na web, desenvolvido para atrair uma ampla audiência, permitindo aos jogadores com diferentes gostos pessoais experimentar o jogo à sua própria maneira. O jogo apresenta um mundo aquático abstrato que convida o jogador a mergulhar nele, aprender, explorar e, obviamente, sobreviver...
Para você que gosta de Teoria da Evolução, "o forte se alimenta do mais fraco", etc, esse é o jogo perfeito. Com uma música suave, controles baseados em uso do mouse, e baixíssimo tempo de aprendizado, flOw pode te deixar vidrado na tela do computador por horas.


